研究内容
① 【創薬研究】エピジェネティックス x 創薬研究 → 新規治療薬開発
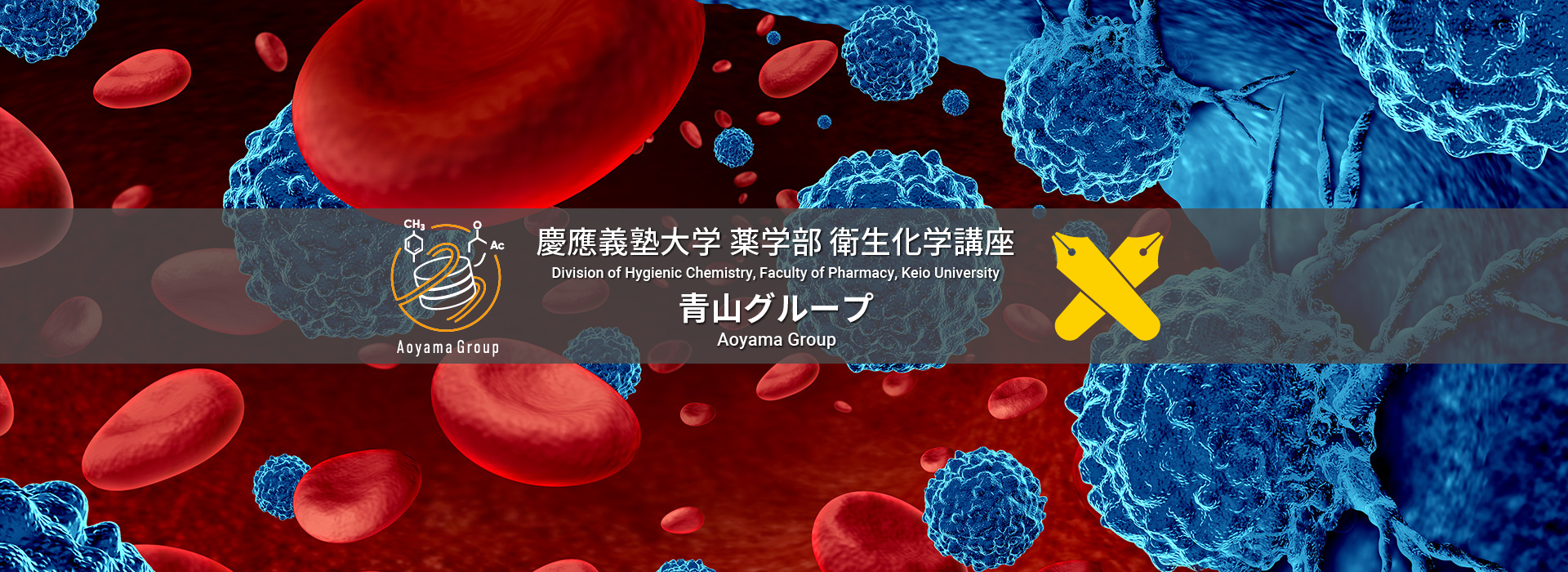
細胞の中では、必要な遺伝子だけが正しく使われるよう、精密な制御が行われています。その中心的な仕組みの一つが、ポリコーム抑制複合体(PRC2)による遺伝子発現制御です。PRC2の酵素サブユニットであるEZH2は、転写を抑えるヒストン修飾 H3K27me3 を付加する主要な酵素であり、その異常は骨髄異形成症候群(MDS)などの重篤な血液がんと深く関係しています。私たちは、EZH2の機能が失われたMDSのマウスモデルを用いて研究を行い、これまで見過ごされがちであったEZH1が、疾患の維持に不可欠であることを明らかにしました。興味深いことに、正常な状態ではEZH1を欠損させても影響は限定的であり、この特徴からEZH1やその制御機構は、副作用の少ない新しい創薬標的として大きな可能性を秘めています。
現在は、BioIDによるプロテオーム解析やCRISPRスクリーニングといった最先端の分子生物学的手法を用いて、EZH1がどのように制御され、どの分子と協調して働いているのかを詳しく解析しています。得られた知見を、将来的な創薬研究へとつなげることが目標です。本研究室では現在、MDSを中心としたPRC2関連がんを主な対象としていますが、将来的には疾患iPS細胞を実験モデルとして導入し、精神疾患(うつ病など)や発達障害(ASD、ADHDなど)といった、社会的関心の高い疾患領域への展開も視野に入れています。
② 【老化研究】エピジェネティックス x 老化研究 → 健康寿命延伸
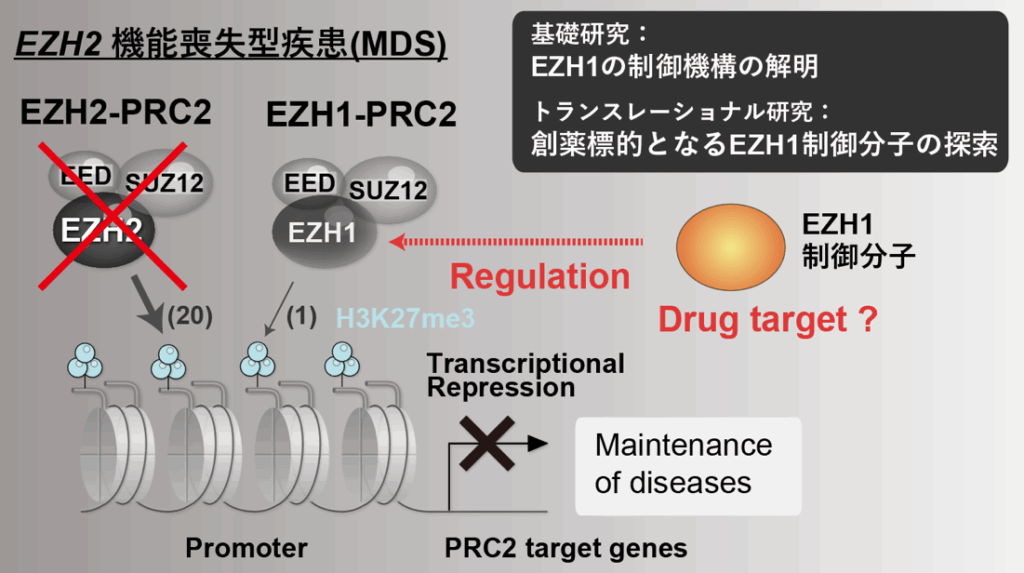
老化は長い間、「誰にも避けられない自然現象」と考えられてきました。しかし近年、老化は治療や介入が可能な生命現象として再定義されつつあり、世界中で注目を集めています。細胞は一定のストレスを受けると増殖を停止し、「老化細胞」と呼ばれる状態になります。老化細胞は単に止まっているだけでなく、SASP(Senescence-Associated Secretory Phenotype)と呼ばれる炎症性物質を分泌し、周囲の組織に慢性炎症や老化を広げることで、がんや生活習慣病などの加齢性疾患の発症を促進します。
当グループでは、老化細胞と正常細胞の違いをエピジェネティックス(ヒストン修飾)の視点から解析し、老化細胞を選択的に除去するセノリシス薬や、SASPを制御する新しい介入戦略の開発を目指しています。老化細胞を標的として制御できれば、がんを含む多くの老化関連疾患の予防につながる可能性があります。さらに私たちは、「エピジェネティックメモリー」と呼ばれるクロマチン修飾の“記憶”にも注目しています。高齢個体の細胞には、長い時間をかけて蓄積されたヒストン修飾の痕跡が存在すると考えられます。これらを詳細に解析することで、老化がどのように細胞に刻み込まれていくのか、その仕組みを分子レベルで理解しようとしています。老化を「仕方のないもの」として受け入れるのではなく、制御し、介入し、健康寿命を延ばす。本研究室では、そんな挑戦的なテーマに、最先端の分子生物学とエピジェネティクスを用いて取り組んでいます。
③ 【食品科学】エピジェネティックス x 食品科学 → 健康寿命延伸
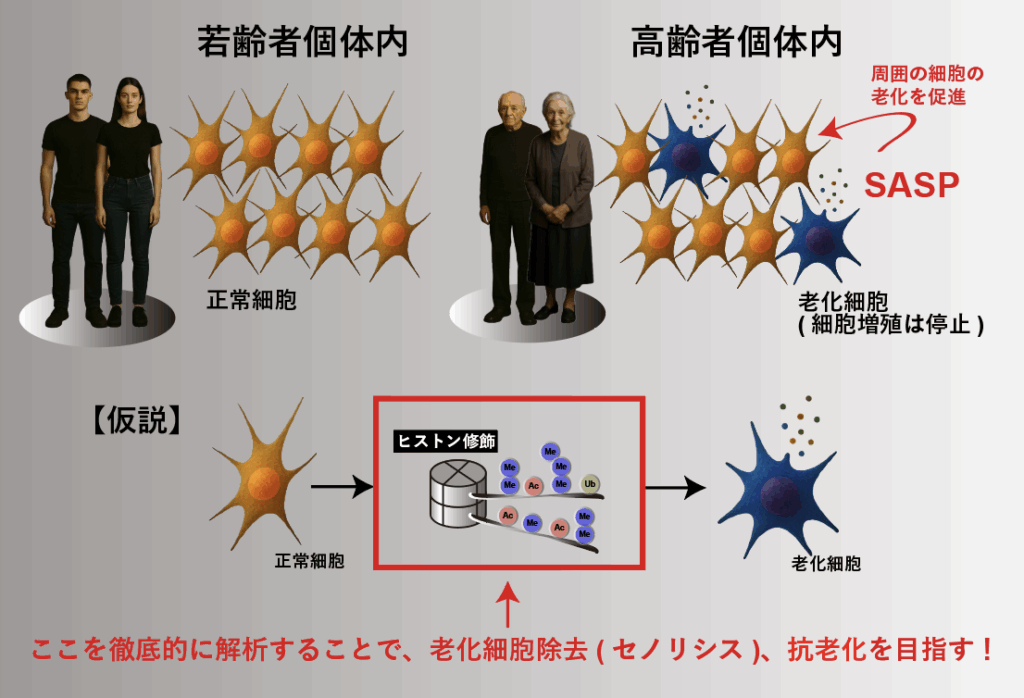
コーヒー摂取は、長寿や心血管疾患リスクの低下、糖尿病予防など、多様な健康効果が疫学的に報告されています。一方で、なぜコーヒーが体に良いのか、その分子レベルの仕組みには、まだ多くの謎が残されています。コーヒーはカフェインだけでなく非常に多くの成分を含み、さらに焙煎という工程を経ることで成分が変化します。この「成分の多様性」と「動的な変化」を併せ持つ点こそが、コーヒー研究の面白さであり、無限の未知の可能性が広がる理由です。私たちは、エピジェネティックス(ヒストン修飾)という視点からコーヒーの作用に注目し、コーヒー処理によって多数のヒストン修飾が大きく変化することを見出しました。これらの中には、健康や寿命との関係が報告されているヒストン修飾も含まれており、コーヒーが私たちの体の「遺伝子の使われ方」を調節している可能性が示唆されます。
本グループでは、こうした基礎研究の発見を出発点として、コーヒーという身近な嗜好品が、どのように健康や老化に影響するのかを分子レベルで解き明かすことを目指しています。将来的には、ヒストン修飾を標的とした薬剤との組み合わせや、健康寿命の延伸につながる新しい予防医療の考え方へと発展させていきます。
④【その他】
がんに関連する分子ネットワークの解明を進めています。近接依存的ビオチン化法(TurboID-BioID)を用いて相互作用分子を網羅的に解析することにより、AKT/mTORシグナル活性化やアポトーシス制御との新規な関連性を明らかにしつつあります。これにより、ALK陽性リンパ腫をはじめとするがん細胞の増殖や生存優位性を支える仕組みの一端を提示しています[Higashi et al., J Biochem. 2025]。
⑤【共同研究】
共同研究も展開しており、疾患発症メカニズムの理解、創薬研究、新規治療戦略への応用を目指しています。